Dược Hậu Giang cùng nhiều doanh nghiệp bị thu hồi mỹ phẩm chứa Miconazole
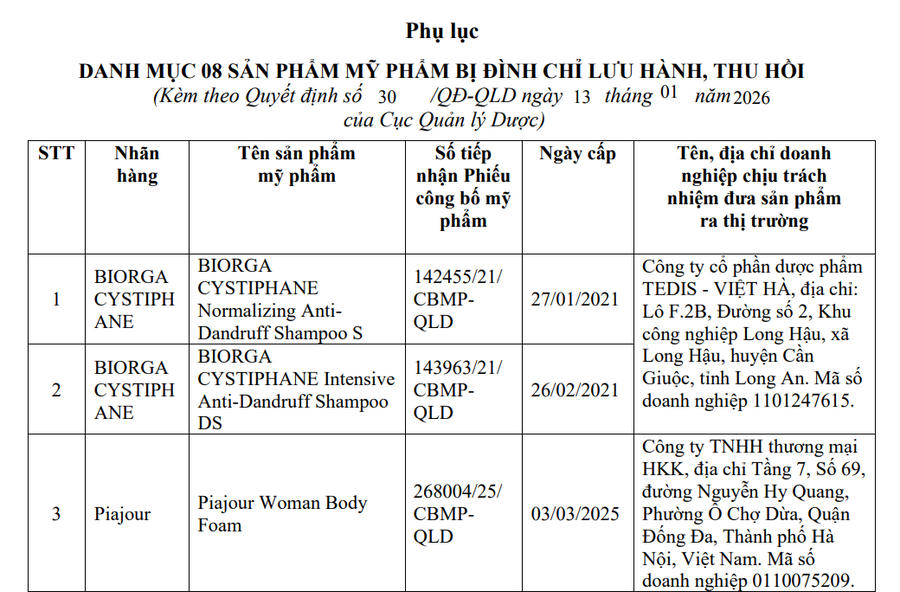
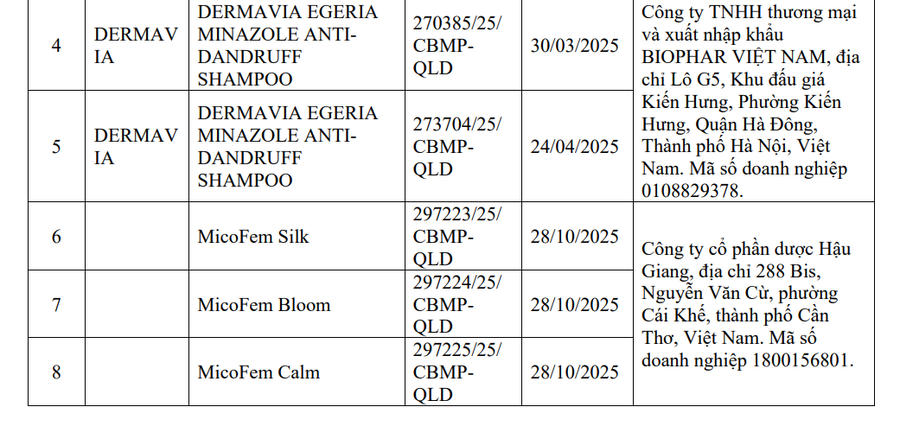
Cục Quản lý Dược (Bộ Y tế) vừa ban hành Quyết định số 30/QĐ-QLD về việc đình chỉ lưu hành và thu hồi trên toàn quốc 8 sản phẩm mỹ phẩm có chứa hoạt chất Miconazole và Miconazole nitrate.

Theo Cục Quản lý Dược, việc đình chỉ lưu hành và thu hồi các sản phẩm nêu trên nhằm tuân thủ quy định của Hiệp định ASEAN về mỹ phẩm, căn cứ Kết luận của Hội đồng Mỹ phẩm ASEAN tại kỳ họp lần thứ 42 diễn ra vào tháng 11/2025, cùng Biên bản họp Hội đồng Khoa học Mỹ phẩm ASEAN lần thứ 42 tổ chức tại Jakarta (Indonesia). Theo kết luận của các cơ quan chuyên môn ASEAN, các sản phẩm mỹ phẩm có chứa Miconazole và Miconazole nitrate không còn phù hợp để tiếp tục lưu hành trong nhóm mỹ phẩm.
Danh mục bị thu hồi bao gồm các sản phẩm dầu gội, bọt vệ sinh và dung dịch vệ sinh do bốn doanh nghiệp chịu trách nhiệm đưa ra thị trường. Trong đó có ba sản phẩm MicoFem Silk, MicoFem Bloom và MicoFem Calm của Công ty CP Dược Hậu Giang; sản phẩm Piajour Woman Body Foam của Công ty TNHH Thương mại HKK; hai sản phẩm Dermavia Egeria Minazole Anti-Dandruff Shampoo do Công ty TNHH Thương mại và Xuất nhập khẩu BIOPHAR Việt Nam phân phối; cùng hai sản phẩm mang nhãn hiệu Biorga Cystiphane do Công ty CP Dược phẩm TEDIS - Việt Hà chịu trách nhiệm.
Cục Quản lý Dược yêu cầu các doanh nghiệp có sản phẩm bị đình chỉ phải khẩn trương gửi thông báo thu hồi đến toàn bộ các cơ sở phân phối, kinh doanh và sử dụng; tiếp nhận các sản phẩm bị trả lại, tổ chức thu hồi và tiêu hủy toàn bộ số sản phẩm còn lưu hành trên thị trường. Báo cáo kết quả thu hồi, tiêu hủy phải được gửi về Cục Quản lý Dược trước ngày 12/2/2026.
Đối với Sở Y tế các tỉnh, thành phố, Cục Quản lý Dược đề nghị thông báo rộng rãi để các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn ngừng ngay việc buôn bán, sử dụng các sản phẩm nằm trong danh mục bị đình chỉ, đồng thời yêu cầu trả lại cho đơn vị cung ứng. Các địa phương có trách nhiệm tăng cường kiểm tra, giám sát, xử lý nghiêm các tổ chức, cá nhân vi phạm theo quy định và báo cáo kết quả thực hiện về Cục Quản lý Dược.
Riêng Sở Y tế Hà Nội, Cần Thơ và Tây Ninh được giao trực tiếp giám sát các doanh nghiệp có trụ sở trên địa bàn trong quá trình thu hồi, tiêu hủy sản phẩm; báo cáo kết quả kiểm tra, giám sát về Cục Quản lý Dược trước ngày 02/3/2026.










